Инструкция
1
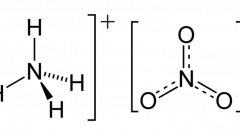
В природе азот находится в свободном состоянии, а также в составе некоторых соединений. В промышленности его получают из жидкого воздуха. Азот является одним из самых распространенных газов, он не имеет цвета и запаха. По химическим свойствам азот считается окислителем, поэтому соединяется с некоторыми металлами. Правда, при комнатной температуре он реагирует лишь с литием, а с другими металлами азот способен вступать в реакцию лишь при нагреве. Чаще всего в природе встречается азот N2. Он способен образовывать различные соединения и легко вступает в реакции. Подавляющее большинство соединений азота применяется для изготовления удобрений и инсектицидов.
2
Продуктом реакции азота с водородом является такое соединение, как аммиак. Аммиак представляет собой бесцветный газ, молекула которого состоит из одного атома азота и трех атомов водорода. Он имеет резкий запах. Данное вещество обладает уникальными свойствами, и вследствие этого находит широкое применение в промышленности и сельском хозяйстве. Соединяясь с водой, аммиак образовывает раствор, именуемый аммиачной водой. В быту раствор аммиака чаще называется нашатырным спиртом. Получают его с помощью следующей реакции:NH3 + H2O = NH4OHNH4OH - это и есть нашатырный спирт, который также называют гидроксидом аммония. Поскольку аммиак обладает восстановительными способностями, аммиачный раствор имеет слабощелочную реакцию.
3
В промышленности аммиак получают путем его синтеза из азота и водорода. Так как реакция обратима и является экзотермической, то она записывается следующим образом:N2 +3H2 = 2NH3 +?H, где ?H = -92,4 кДжПротекает эта реакция в присутствии пористого железа с оксидом алюминия или кальция. Проводят ее при температуре от 500 до 600 °C. На качество получения аммиака, кроме температуры, также влияет отсутствие в сырье примесей. Поэтому перед началом реакции из азота и водорода удаляют воду, оксиды углерода, и, особенно, сернистые соединения.
4
В лабораторных условиях аммиак получают путем нагревания хлорида аммония и гашеной извести:2NH4Cl + Ca(OH)2 = CaCl2 + 2NH3 + 2H2OВ ходе реакции выпадает в осадок вещество белого цвета - соль CaCl2, выделяется вода, а также вырабатывается аммиак, который и требуется получить.Другой лабораторный способ получения аммиака заключается в кипячении аммиачной воды и осушении полученного пара.
Видео по теме
Обратите внимание
Аммиак токсичен как для человека, так и для животных. Особенно опасен жидкий аммиак. Поэтому при использовании аммиака нужно соблюдать осторожность. Храните аммиачные удобрения подальше от детей и домашних питомцев. Нельзя также вдыхать пары аммиака при проведении опытов.