Инструкция
1
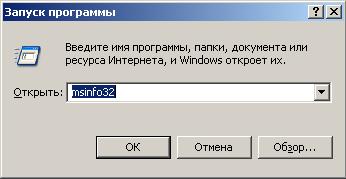
На вашем рабочем столе щелкните мышкой кнопку «Пуск» и выберите пункт «Выполнить…». Откроется диалоговое окно запуска программ. В поле «Открыть» введите название утилиты - msinfo32. Нажмите клавишу «Enter».
2
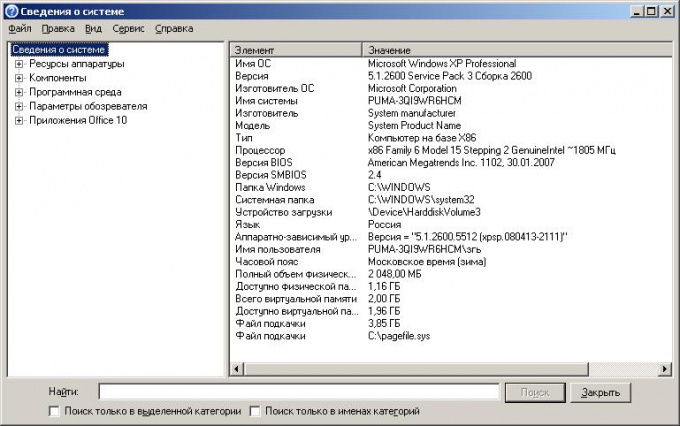
На экране покажется окно «Сведения о системе», где представлена полная информация о вашем компьютере. В левой части данного окна представлен список-дерево ресурсов и подключенных устройств компьютера. Справа расположено окно, где выводятся данные о выбранном устройстве или ресурсе.
3
Выберите слева в списке верхнюю строку «Сведения о системе». Справа тут же отобразится общая информация о конфигурации вашего компьютера.
4
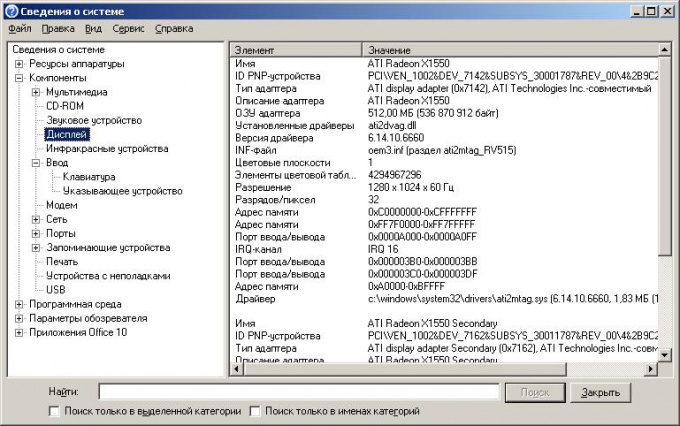
Для более детальной информации по конкретному устройству в левой части окна, в списке-дереве, выделите соответствующую строку. Нужные данные покажутся в правой половине окна в полях «Элемент» и «Значение».
5
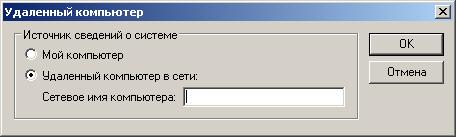
Если необходимо узнать конфигурацию удаленного компьютера, входящего в общую локальную сеть, выберите пункты основного меню: «Вид» - «Удаленный компьютер…». Введите имя компьютера в открывшееся поле. Нажмите кнопку «Ок». В окне отобразятся сведения об удаленном ПК.
Видео по теме
Источники:
- Определение электронной конфигурации внешнего